理科【基本】物質の溶解
問1 溶解
(1)□ に当てはまる語句を答えなさい。
① 溶解とは、物質が液体に \(\boxed{ア}\) に溶けて \(\boxed{イ}\) な溶液になることである。
- 答え(1)- ①
- ア:一様(均一) イ:透明
- 解説(1)- ①
- 物質が液体に一様(均一)に溶ける:溶液全体が同じ濃さになっている状態
透明:透き通っていること。向こう側が見える。
溶液には無色(色がない)のものと、色がついているものがある。
② 水に物質が溶けた液体を □ という。
- 答え(1)- ②
- 水溶液
- 解説(1)- ②
- 【水溶液の条件】
① 透明で溶けているものを見ることができない。
② 1 つの容器の中ではどこでも濃さは同じである。
③ ろ過しても溶けている物質を取り出すことはできない。
③ 溶液に溶けているものを \(\boxed{ア}\)、物質を溶かしているものを \(\boxed{イ}\) という。
- 答え(1)- ③
- ア:溶質 イ:溶媒
- 解説(1)- ③
- 砂糖を水に溶かした砂糖水の場合
溶液 = 砂糖水
溶質 = 砂糖
溶媒 = 水
④ 溶液の濃さ(濃度)は、溶液全体の重さに対する溶質の重さの割合である。ふつうは、全体を 100 としたときの割合であるパーセント [%] で表され、次の式で求めることができる。
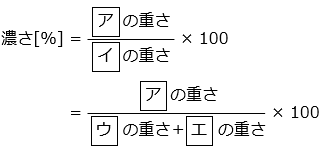
- 答え(1)- ④
- ア:溶質 イ:溶液 ウ:溶質 エ:溶媒
(ウ、エは順不同)
- 解説答え(1)- ④
- 【水溶液の濃さ(濃度)の求め方】
濃度 [%] = \(\dfrac{溶質の重さ}{溶液の重さ}\) × 100
溶液の重さ = 溶質の重さ + 溶媒の重さ
(2)溶かす前の水と食塩の重さの合計は、食塩水の重さと比べるとどのようになっていますか。ア~ウから 1 つ選んで答えなさい。
ア. 軽い
イ. 同じ
ウ. 重い
- 答え(2)
- イ
- 解説(2)
- 溶かす前と後で、重さは変わらない。
溶液の重さ = 溶質の重さ + 溶媒の重さ、すなわち、食塩水の重さ = 食塩の重さ + 水の重さ
(3)水と食塩の溶かす前の体積の合計は、食塩水の体積と比べるとどのようになっていますか。ア~ウから 1 つ選んで答えなさい。
ア. 小さい
イ. 同じ
ウ. 大きい
- 答え(3)
- ウ
- 解説(3)
- 食塩水では、食塩の粒が水のすき間に入り込むため混ぜる前より体積は小さくなります。したがって、溶かす前のほうが大きい。
問2 溶解度
(1)一定量( 100 g )の水に対して溶ける溶質の限度量を表す数値を何といいますか。
- 答え(1)
- 溶解度
- 解説(1)
- 物質には、
・まったく溶けないもの
・溶ける限度のあるもの
・無制限に溶けるもの
がある。
(2)水に対して溶質を限度いっぱいまで溶かした水溶液を何といいますか。
- 答え(2)
- 飽和水溶液
(3)温度よる溶解度の違いについて、□ に当てはまる語句を答えなさい。
① 固体が水に溶けるとき、ふつう、水温が □ なるほどよく溶ける。
- 答え(3)- ①
- 高く
- 解説(3)- ①
- 例外:水酸化カルシウム(消石灰)は低温のほうが溶ける。
② 気体が水に溶けるとき、気圧が \(\boxed{ア}\) ほうがよく溶け、水温が \(\boxed{イ}\) ほうがよく溶ける。
- 答え(3)- ②
- ア:高い イ:低い
- 解説(3)- ②
- 二酸化炭素を溶かした炭酸飲料のふたを開けると、あわがたくさんでてきます。これは容器の中で気体を溶かしこんでいた大きな圧力が、ふたを開けることで空気中の圧力(大気圧)と同じになるため、溶けきれなくなった二酸化炭素が出てくるからです。
(4)溶質が固体の水溶液から溶質を取り出す方法には、以下に示す A、B の 2 つがあります。①、② の場合、どちらの方法が適しているか記号で答えなさい。
方法 A:飽和水溶液の温度を下げる
方法 B:飽和水溶液の溶媒を減らす
① ホウ酸のように、温度のちがいによって溶解度に大きな差がある場合
② 食塩のように、温度がちがっても溶解度があまり変わらない場合
- 答え(4)
- ① A ② B
- 解説(4)
- ① 温度のちがいによって溶解度に大きな差がある場合、高温の飽和水溶液の温度を下げると、溶けきれなくなった溶質が固体となって出てきます。
② 温度がちがっても溶解度があまり変わらない場合、水を蒸発させると、溶けきれなくなった溶質が固体となって出てきます。
- 固体・液体・気体の溶解度
- 溶解度:一定量 ( 100 g ) の水に対して溶ける溶質の限度量 ( [g] ) を表す数値
【固体の溶解度】
| 温度[℃] 溶質 | 0 | 20 | 40 | 60 | 80 | 100 |
| ホウ酸 | 2.8 | 4.9 | 8.9 | 14.9 | 23.5 | 38.0 |
| 食塩 | 35.6 | 35.8 | 36.3 | 37.1 | 38.0 | 39.3 |
| 砂糖 | 179 | 204 | 238 | 287 | 362 | 485 |
| みょうばん | 3 | 5.9 | 11.7 | 24.8 | 71 | 119 |
| 水酸化カルシウム | 0.14 | 0.13 | 0.11 | 0.09 | 0.07 | 0.05 |
【気体の溶解度】
(「-」はほとんど溶けないことを表す )
| 温度[℃] 溶質 | 0 | 20 | 40 | 60 | 80 | 100 |
| アンモニア | 1176 | 702 | – | – | – | – |
| 塩化水素 | 507 | 442 | 386 | 339 | – | – |
| 塩素 | 4.61 | 2.30 | 1.44 | 1.02 | 0.68 | 0.00 |
| 二酸化硫黄 | 80 | 39 | 19 | – | – | – |
| 二酸化炭素 | 1.71 | 0.88 | 0.53 | 0.36 | – | – |
| 酸素 | 0.049 | 0.031 | 0.023 | 0.019 | 0.018 | 0.017 |
【液体の溶解度】
・無制限に溶けるもの:アルコール、酢酸、グリセリン、過酸化水素など
・溶ける限度のあるもの:エチルエーテル、クレゾールなど
・まったく溶けないもの:油、水銀など
問3
食塩水から結晶を取り出すために次の操作 I、II を行いました。
【操作 I】器具 A を使ってはかりとった食塩を、器具 B ではかりとった 20 ℃ の水 50 mL にとかして飽和食塩水を作った。
【操作 II】操作 I の食塩水を( ア )させて、多くの結晶を得た。
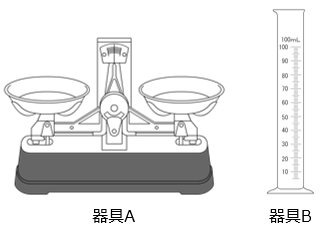
表 100 g の水にとける食塩の量
| 温度[℃] | 0 | 20 | 40 | 60 | 80 | 100 |
| 食塩[g] | 35.7 | 35.8 | 36.3 | 37.1 | 38.0 | 39.3 |
(1)器具 A、B の名前を答えなさい。
- 答え(1)
- A:上皿てんびん B:メスシリンダー
(2)青字部分の食塩水をつくるために必要な食塩は何 g ですか。ここで、20 ℃ の水 1 mL の重さは 1 g とします。
- 答え(2)
- 17.9 g
- 解説(2)
- 表より 20 ℃ の水 100 g にとける食塩の量は 35.8 g である。よって、水 50 mL ( = 50 g ) にとける食塩の量は、
35.8 ÷ 2 = 17.9 [g]
(3)操作 II の( ア )の方法としてふさわしいのはどちらですか。また、その理由を答えなさい。
① 氷水で十分に冷却
② 加熱して水を蒸発
- 答え(3)
- ②
理由:氷水で 0 ℃ まで冷却しても 0.5 g しか結晶にならないが、加熱して水を蒸発させるともっと多くの結晶を得ることができるから。
- 解説(3)
- ① 温度のちがいによって溶解度に大きな差がある場合に有効
② 温度がちがっても溶解度があまり変わらない場合に有効
問4
食塩水やホウ酸水のように、ものが水に溶けたものを水溶液といいます。水溶液について以下の問いに答えなさい。ただし、計算で割り切れないときは、小数第 2 位を四捨五入して数値を書きなさい。
(1)25 g の食塩を 100 g の水に溶かしました。この水溶液の濃度は何 % ですか。
- 答え(1)
- 20 %
- 解説(1)
- 濃度 [%] = \(\dfrac{溶質の重さ}{水溶液の重さ}\) × 100
溶質 = 食塩:25 g
水溶液 = 食塩 + 水:25 + 100 = 125 [g]
\(\dfrac{25}{125}\) × 100 = 20 [%]
(2)10 g の食塩に水を加えて 10 % の濃度の水溶液をつくります。何 g の水を加えればよいですか。
- 答え(2)
- 90 g
- 解説(2)
- 水溶液の重さ = \(\dfrac{溶質の重さ\ ×\ 100}{濃度\ [\%]}\)
まず水溶液全体の重さを求めると、
\(\dfrac{10\ ×\ 100}{10}\) = 100 [g]
よって、加える水の量は、100 – 10 = 90 [g]
(3)ものを水に溶かしたとき、溶ける量(重さ)には限度があります。表は、100 g の水に溶かすことができるホウ酸の重さを示したものです。
| 温度 [℃] | 20 | 40 | 60 |
| ホウ酸の重さ [g] | 5 | 9 | 15 |
① 20 ℃ の水 200 g にホウ酸 8 g を加えてよくかき混ぜました。ホウ酸はすべて溶けますか。「溶ける」または「溶けない」で答えなさい。
- 答え(3)- ①
- 溶ける
- 解説(3)- ①
- 表より、20 ℃ の水 100 g には 5 g のホウ酸が溶けるので、水 200 g には 5 × 2 = 10 [g] のホウ酸を溶かすことができる。よって、8 g のホウ酸は「溶ける」
② 40 ℃ の水 150 g にホウ酸 18 g を加えてよくかき混ぜました。この水溶液の濃度は何 % ですか。
- 答え(3)- ②
- 8.3 %
- 解説(3)- ②
- 表より、40 ℃ の水 100 g には 9 g のホウ酸が溶けるので、水 150 g には 9 × 1.5 = 13.5 [g] のホウ酸を溶かすことができる。つまり、18 g のホウ酸を加えても 13.5 g しか溶けない。
よって、濃度は、
\(\dfrac{13.5}{13.5 + 150}\) × 100
= \(\dfrac{13.5}{163.5}\) × 100 = 8.25… ≒ 8.3 [%]
③ 60 ℃ の水 100 g にホウ酸 21 g を加えてよくかき混ぜると、ホウ酸が溶け残ってしまいました。さらに 60 ℃ の水を少なくとも何 g 加えるとホウ酸は完全に溶けますか。また、このときのホウ酸が完全に溶けた水溶液の濃度は何 % ですか。
- 答え(3)- ③
- 40 g、13.0 %
- 解説(3)- ③
- 表より、60 ℃ の水 100 g には 15 g のホウ酸が溶けるので、ホウ酸 21 g を完全に溶かすために必要な 60 ℃ の水は、
100 × \(\dfrac{21}{15}\) = 140 [g]
よって加える水の量は 140 – 100 = 40 [g]
このときの水溶液の濃度は、水 100 g に 15 g のホウ酸を溶かした濃度と等しい。
\(\dfrac{15}{15 + 100}\) × 100
= \(\dfrac{15}{115}\) × 100 = 13.04… ≒ 13.0 [%]
問5
物質が水に溶ける量について、実験 1 と実験 2 を行いました。
【実験 1】100 g の水の温度を変えながら、5 種類の物質 A ~ E が限界まで溶ける量を調べたところ、下のグラフのようになりました。
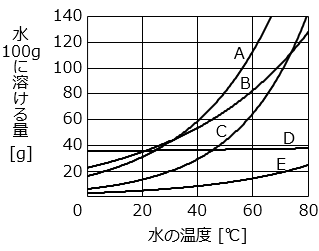
(1)水の温度が 40 ℃ のとき、水 100 g に溶ける量が多い順に、5 種類の物質を並べなさい。
- 答え(1)
- A → B → D → C → E
- 解説(1)
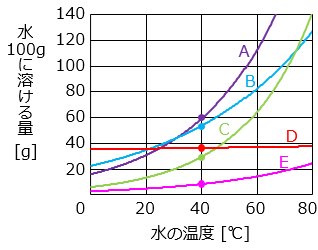
(2)水の温度を 0 ℃ から 40 ℃ に上げたとき、水 100 g に溶ける量がもっとも大きく変化するものは、5 種類のうちどれですか。
- 答え(2)
- A
- 解説(2)
- グラフより、A が 40 g 以上増えていてもっとも大きく変化している。
【実験 2】ホウ酸を、さまざまな温度で 100 g の水に限界まで溶ける量を調べたところ、下の表のようになりました。
| 水の温度 [℃] | 0 | 20 | 40 | 60 | 80 | 100 |
| ホウ酸 [g] | 2.8 | 4.9 | 8.9 | 14.9 | 23.5 | 38.0 |
(3)60 ℃ の水に限界までホウ酸を溶かしました。溶かしたホウ酸が 29.8 g だったとき、この水溶液は何 g になりますか。
- 答え(3)
- 229.8 g
- 解説(3)
- 29.8 g のホウ酸を溶かすために必要な 60 ℃ の水の量は、
\(\dfrac{29.8}{14.9}\) × 100 = 200 [g]
よって水溶液は 29.8 + 200 = 229.8 [g]
(4)40 ℃ の水 330 g に限界までホウ酸を溶かしたとき、ホウ酸の水溶液の濃さは何 % になりますか。小数第 2 位を四捨五入して、小数第 1 位まで求めなさい。
- 答え(4)
- 8.2 %
- 解説(4)
- \(\dfrac{8.9}{8.9\ +\ 100}\) × 100
= \(\dfrac{8.9}{108.9}\) × 100 = 8.17… ≒ 8.2 [%]
※ある温度の飽和水溶液の濃さは、量が変わっても同じである。すなわち、40 ℃ の水 330 g に限界まで溶けるホウ酸の量を求める必要はない。
問6
物質の水への溶け方を調べるために、次の実験 ① ~ ③ を行いました。
【実験】
① ビーカーに、水 100 g と物質 A 60 g を入れてよくかき混ぜたところ、物質 A が溶け残りました。
② かき混ぜながらガスバーナーで加熱して 50 ℃ にしたところ、ビーカー内の物質 A はすべて溶けました。その後、50 ℃ のまま、水溶液を静かに置いておきました。
③ このビーカー内の水溶液を 20 ℃ になるまで冷ましたところ、ビーカー内に物質 A の結晶が出ていました。20 ℃ のまま、ろ過して結晶と水溶液を分けました。
(1)実験 ② の青字部分について、水溶液を静かに置いておいたときの、物質 A がすべて溶けている様子を図で示したものとして最も適切なものを ア ~ エから選びなさい。ただし、図中の「〇」は物質 A の粒子を示しています。
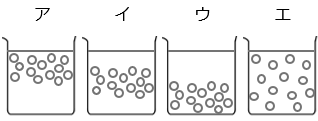
- 答え(1)
- エ
- 解説(1)
- 【水溶液の条件】
① 透明で溶けているものを見ることができない。
② 1 つの容器の中ではどこでも濃さは同じである。
③ ろ過しても溶けている物質を取り出すことはできない。
物質 A と物質 B について、水溶液の温度と 100 g の水に溶ける物質の質量との関係を調べてグラフに表しました。
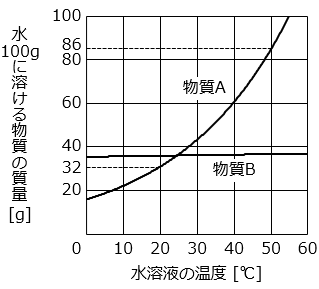
(2)実験 ③ で 20 ℃ になるまで冷やしたときに出ていた物質 A の結晶の質量は全部で何 g ですか。
- 答え(2)
- 28 g
- 解説(2)
- 水溶液が 50 ℃ のとき、このビーカーの水溶液には物質 A は 60 g 溶けている。グラフより、水溶液が 20 ℃ のとき物質 A は 32 g までしか溶けない。
よって出てくる結晶の質量は、
60 – 32 = 28 [g]
(3)実験 ③ でろ過して得られた水溶液の濃度は何 % ですか。小数第一位を四捨五入して整数で答えなさい。
- 答え(3)
- 24 %
- 解説(3)
- このろ液は 20 ℃ の水 100 g に物質 A が 32 g 溶けた水溶液である。
よって濃度は、
\(\dfrac{32}{32 + 100}\) × 100
\(\dfrac{32}{132}\) × 100 = 24.2… ≒ 24 [%]
(4)この実験の物質 A のように、水溶液の温度を下げて水溶液から結晶を取り出す方法は、物質 B には適しません。その理由を、グラフを参考にして「温度」という言葉を使って答えなさい。
- 答え(4)
- 物質 B は、温度が変化しても 100 g の水に溶ける物質の質量がほとんど変化しないから。
- 解説(4)
- 物質 A のように、温度のちがいによって溶解度に大きな差がある場合は、高温の飽和水溶液の温度を下げて、溶けきれなくなった溶質(結晶)を取り出す方法が適している。
一方、物質 B のように、温度がちがっても溶解度があまり変わらない場合は、水を蒸発させて、溶けきれなくなった溶質(結晶)を取り出す方法が適している。
問7
温度をいろいろと変化させた 100 mL の水を用意して、そこに食塩とホウ酸を溶かして、それぞれ何 g まで溶けるかを調べ、下の表にまとめました。
| 水の温度 [℃] | 0 | 20 | 40 | 60 |
| 食塩 [g] | 35.5 | 35.7 | 36.0 | 37.1 |
| ホウ酸 [g] | 2.8 | 4.8 | 8.7 | 14.8 |
(1)水の温度が上がるにつれて、溶ける量が大きく変化しているのは、食塩とホウ酸のどちらですか。
- 答え(1)
- ホウ酸
- 解説(1)
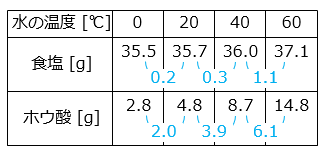
(2)60 ℃ の水 150 mL には、ホウ酸は何 g まで溶けますか。
- 答え(2)
- 22.2 g
- 解説(2)
- 60 ℃ の水 100 mL には 14.8 g まで溶けるので、
14.8 × \(\dfrac{150}{100}\)
= 14.8 × \(\dfrac{3}{2}\) = 22.2 [g]
(3)(2)の水溶液を 20 ℃ まで冷やすと、ホウ酸の結晶を何 g 取り出せますか。
- 答え(3)
- 15.0 g
- 解説(3)
- 20 ℃ の水 100 mL には 4.8 g まで溶けるので、150 mL に溶けるホウ酸の量は、
4.8 × \(\dfrac{150}{100}\)
= 4.8 × \(\dfrac{3}{2}\) = 7.2 [g]
よって取り出せる結晶の量は、
22.2 – 7.2 = 15.0 [g]
※表中の値は小数第一位まで書かれているので、答えの値は整数であっても小数第一位まで書く!
問8
水にいろいろなものを入れた場合、溶けるものと溶けないものがあります。たとえば、砂や鉄粉は水の中に入れても見えますが、食塩や砂糖は水に入れると溶けて見えなくなります。このときの透明になった液体を水溶液といいます。
(1)水の中に砂糖を入れたときの説明として正しいものを次のア~オから 1 つ選んで答えなさい。
ア. 砂糖は見えなくなったので、水の中には残っていない。
イ. 砂糖が水に溶けるのは、水より軽いからである。
ウ. 溶けて見えなくなってしまった砂糖は、あとで取り出すことができる。
エ. 溶けるということは砂糖が水の中にある気泡(空気の泡)の中に入ることである。
オ. 100 g の水に 5 g の砂糖を溶かして透明になると、重さは 100 g になる。
- 答え(1)
- ウ
- 解説(1)
- ア:見えなくなっても、砂糖は水の中にちゃんとある。⇒ ×
イ:溶けるかどうかは重さでは決まらない。⇒ ×
ウ:水を蒸発させると、砂糖を取り出すことができる。⇒ 〇
エ:砂糖の粒子は水の中に均一に広がっている。⇒ ×
オ:水溶液の重さは溶質(砂糖)と溶媒(水)の和。よって、5 + 100 = 105 [g] になる。⇒ ×
グラフは、食塩とミョウバンの水に対する溶解度を表したものです。このグラフは、100 g の水に溶ける量を表しています。
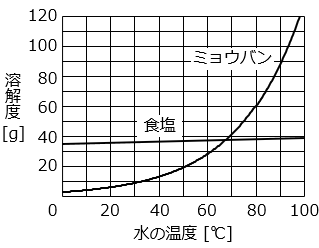
(2)溶解度の説明として正しくないものを、次のア~オから 1 つ選んで答えなさい。
ア. 溶解度はものの種類によって異なる。
イ. 溶解度は同じものでも温度によって異なる。
ウ. 水の量を増やしても溶解度は変わらない。
エ. ものの粒を小さくしても溶解度は変わらない。
オ. よくかき回すと溶解度は上がる。
- 答え(2)
- オ
- 解説(2)
- ア、イ:グラフより。⇒ 〇
ウ:溶解度は「水100 gにどれだけ溶けるか」という決まった量でなので、水の量を増やしても、基準は 100 gなので数値は変わらない。⇒ 〇
エ:粒を細かくすると早く溶けるようにはなるが、溶ける量の限界(溶解度)は同じ。⇒ 〇
オ:かき回すと溶ける速さは速くなるが、溶ける量の限界(溶解度)は同じ。⇒ ×
(3)食塩とミョウバンの飽和水溶液を、50 ℃ の水 100 g を用いてそれぞれ作りました。それらの重さにはおよそ何 g の差がありますか。次のア~オよりもっとも近い値を 1 つ選んで答えなさい。
ア. 8 g
イ. 13 g
ウ. 18 g
エ. 23 g
オ. 28 g
- 答え(3)
- ウ
- 解説(3)
- 水の量は同じなので、飽和水溶液の重さの差は溶けている食塩とミョウバンの重さの差に等しい。
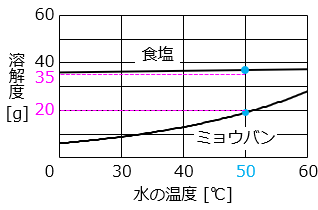
グラフより、15 g より大きく 20 g より小さい
(4) 90 ℃ の水 100 g で作ったミョウバンの飽和水溶液の濃度はおよそ何 % ですか。整数で答えなさい。
- 答え(4)
- 47 %
- 解説(4)
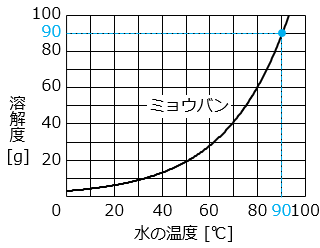
グラフより、90 ℃ のときのミョウバンの溶解度は約 90 g より、
\(\dfrac{90}{90\ +\ 100}\) × 100
= \(\dfrac{90}{190}\) × 100 = 47.3… ≒ 47 [%]
(5) (4)で作った飽和水溶液を 20 ℃ まで冷やしていくと、およそ何 g のミョウバンの結晶が出てきますか。整数で答えなさい。
- 答え(5)
- 85 g
- 解説(5)
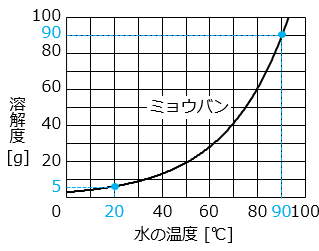
グラフより、90 ℃ のときのミョウバンの溶解度は約 90 g、20 ℃ のときは約 5 g なので、
90 – 5 = 85 [g]
(6)20 ℃ の水 100 g で作ったミョウバンの飽和水溶液と、90 ℃ の水 200 g で作ったミョウバンの飽和水溶液を 1 つのビーカーに入れてかき混ぜたのち、50 ℃ になるまで十分に待ちました。このとき、およそ何 g のミョウバンが結晶になって出てきますか。
- 答え(6)
- 125 g
- 解説(6)
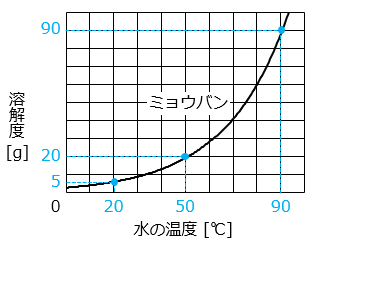
グラフより、20 ℃ の水 100 g に溶けているミョウバンは約 5 g、90 ℃ の水 200 g に溶けているミョウバンは約 90 × 2 = 180 [g] である。
よって、これらの飽和水溶液を混ぜた水溶液は、水 300 g 中に約 180 + 5 = 185 [g] のミョウバンが溶けていると考えられる。
50 ℃ の水 300 g に溶かすことができるミョウバンは約 20 × \(\dfrac{300}{100}\) = 60 [g] である。
よって、出てくる結晶のおよその量は、185 – 60 = 125 [g]
問9
水に溶けるミョウバンの量が、水の量と温度によってどのように変わるのかを調べるために、次のような実験を行いました。
【手順 1】
5 つのビーカー A ~ E を用意し、表のように A ~ C には 0 ℃ の水を 30 ~ 120 g、D と E には 20 ℃ と 40 ℃ の水を 30 g ずつ入れました。
【手順 2】
ビーカー A ~ E に、ミョウバンを 10 g ずつ加えてよくかき混ぜると、どれもミョウバンは溶けきらず、ビーカーの底に残りました。
【手順 3】
それぞれのビーカーで溶け残ったミョウバンをろ過し、その重さをてんびんではかったところ、表のような結果になりました。
| ビーカー | A | B | C | D | E |
| 水 | 0 ℃ | 0 ℃ | 0 ℃ | 20 ℃ | 40 ℃ |
| 30 g | 60 g | 120 g | 30 g | 30 g |
溶け残った
ミョウバン | 8.8 g | 7.6 g | 5.2 g | 7.9 g | 6.0 g |
(1)表の結果からわかることとして正しいものを、ア~エから 1 つ選びなさい。
ア. 水の量が少なく、温度が低くなるほど、溶けるミョウバンの量は多くなる。
イ. 水の量が少なく、温度が高くなるほど、溶けるミョウバンの量は多くなる。
ウ. 水の量が多く、温度が低くなるほど、溶けるミョウバンの量は多くなる。
エ. 水の量が多く、温度が高くなるほど、溶けるミョウバンの量は多くなる。
- 答え(1)
- エ
- 解説(1)
- 固体が水に溶けるとき、水の量が多く、温度が高くなるほどよく溶ける。
例外:水酸化カルシウム(消石灰)は低温のほうがよく溶ける。
(2)ビーカー A ~ E の水溶液のうち、最も濃いのはどれですか。
- 答え(2)
- E
- 解説(2)
- ビーカー A ~ E はすべてミョウバンが溶け残っていることから、水溶液は飽和水溶液になっている。よって、同じ温度( A ~ C )では水の量に関わらず、濃さはすべて等しい。同じ水の量( A, D, E )では温度が高いほど多く溶けるため、E の水溶液が最も濃い。
(3)ビーカー B において、ろ過した後の水溶液の重さは何 g ですか。
- 答え(3)
- 62.4 g
- 解説(3)
- 0 ℃ の水 60 g に溶けているミョウバンの量は、
10 – 7.6 = 2.4 [g]
よって、60 + 2.4 = 62.4 [g]
(4)ビーカー C において、ろ過する前に 0 ℃ の水を 20 g 足してよくかき混ぜると、溶け残るミョウバンは何 g になりますか。
- 答え(4)
- 4.4 g
- 解説(4)
- (3)より、0 ℃ の水 60 g に溶けるミョウバンの量は 2.4 g なので、0 ℃ の水 20 g に溶けるミョウバンの量は、
2.4 ÷ 3 = 0.8 [g]
ビーカー C において、ろ過する前に 0 ℃ の水を 20 g 足すとさらに 0.8 g溶けるので、溶け残るミョウバンは、
5.2 – 0.8 = 4.4 [g]
(5)ビーカー D において、ろ過した水溶液を 0 ℃ まで下げると結晶が出てきました。このとき出てきた結晶は何 g ですか。
- 答え(5)
- 0.9 g
- 解説(5)
- ビーカー D( 20 ℃, 30 g )に溶けているミョウバンの量は、
10 – 7.9 = 2.1 [g]
0 ℃ の水 30 g( ビーカー A )に溶けるミョウバンの量は、
10 – 8.8 = 1.2 [g]
よって出てきた結晶は、2.1 – 1.2 = 0.9 [g]
(6)60 ℃ の水 50 g にミョウバン 15 g を加えてよくかき混ぜたところ、溶けきらなかったのでろ過しました。ろ過した水溶液を 0 ℃ まで下げると、10.4 g の結晶が出てきました。60 ℃ の水 50 g に溶けたミョウバンは何 g ですか。
- 答え(6)
- 12.4 g
- 解説(6)
- 0 ℃ の水 50 g に溶けるミョウバンの量は、
1.2 × \(\dfrac{50}{30}\) = 2 [g]
60 ℃ の水 50 g に溶けていたミョウバンは、
2 + 10.4 = 12.4 [g]
問10
表はいろいろな温度の水 100 g に溶けるホウ酸と食塩、ミョウバンの限度量を表したものです。
| 水温 [℃] | 20 | 40 | 60 | 80 |
| ホウ酸 [g] | 4.9 | 8.8 | 14.9 | 23.5 |
| 食塩 [g] | 35.8 | 36.3 | 37.1 | 38.0 |
| ミョウバン [g] | 11.4 | 23.8 | 57.4 | 321.6 |
(1)80 ℃ の水 150 g に食塩 50 g を溶かしました。この食塩水の濃さは何 % ですか。
- 答え(1)
- 25.0 %
- 解説(1)
- 80 ℃ の水 150 g に溶ける食塩の限度量は、
38 × \(\dfrac{150}{100}\) = 57 [g]
したがって、食塩 50 g は 80 ℃ の水 150 g に完全に溶ける。よってその濃さは、
\(\dfrac{50}{50\ +\ 150}\) × 100 = 25 [%]
(2)(1)の食塩水には、さらに何 g の食塩を溶かすことができますか。
- 答え(2)
- 7.0 g
- 解説(2)
- 57 – 50 = 7 [g]
(3)80 ℃ の水 150 g にある重さのホウ酸を溶かし、40 ℃ まで冷やすと、ホウ酸の結晶ができました。このホウ酸の結晶をろ過して取り出し、重さを測ると 17.3 g でした。
① ホウ酸の結晶の形として最も適切なものをア~ウから 1 つ選びなさい。
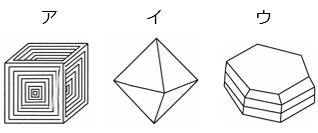
- 答え(3)- ①
- ウ
- 解説(3)- ①
- 食塩(ア):立方体(サイコロ型)
ミョウバン(イ):正八面体
ホウ酸(ウ):六角板状(うすい六角形)
② 80 ℃ の水 150 g に加えたホウ酸の重さは何 g ですか。
- 答え(3)- ②
- 30.5 g
- 解説(3)- ②
- 40 ℃ の水 150 g に溶けるホウ酸の量は、
8.8 × \(\dfrac{150}{100}\) = 13.2 [g]
80 ℃ の水 150 g に加えたホウ酸は、
13.2 + 17.3 = 30.5 [g]
(4)60 ℃ の水にミョウバンを溶けるだけ溶かしたミョウバンの水溶液 200 g を 20 ℃ まで冷やすとミョウバンの結晶ができました。このミョウバンの結晶の重さは何 g ですか。小数第 2 位を四捨五入して答えなさい。
- 答え(4)
- 58.5 g
- 解説(4)
- 60 ℃ の水にミョウバンを溶けるだけ溶かした水溶液(飽和水溶液)200 g 中のミョウバンの重さは、
\(\dfrac{57.4}{57.4\ +\ 100}\) × 200 = 72.935… ≒ 72.94 [g]
すなわち水の重さは、200 – 72.94 ≒ 127.06 [g]
20 ℃ の水 127.06 g に溶けるミョウバンの限界量は、
11.4 × \(\dfrac{127.06}{100}\)
≒ 11.4 × 1.27 ≒ 14.478… ≒ 14.48 [g]
よってできたミョウバンの結晶の重さは、
72.94 – 14.48 = 58.46 ≒ 58.5 [g]













